Lobhudelei für eine unbewiesene Gentherapie
Würden Sie sich ein Loch in den Schädel bohren und in einer diffizilen, 12- bis 18-stündigen Operation sechs Spritzen tief ins Gehirn verabreichen lassen? Mit einer völlig neuen Gentherapie?
Mindestens 20 Personen in den USA und weitere in Europa haben das in einem Experiment an sich machen lassen. Es zeigt, wie verzweifelt sie sein müssen – oder wie hoffnungsvoll. Gemeinsam ist ihnen, dass sie an Chorea Huntington leiden, einer seltenen erblichen Erkrankung, gegen die es bis jetzt kein Mittel gibt.
Falls diese Behandlung wirksam wäre, würde sie das Schicksal von Zehntausenden von Familien zum Positiven wenden. Die «NZZ» berichtete letzten Oktober: «Zum ersten Mal haben Forscher Menschen mit der schweren erblichen Krankheit Huntington erfolgreich behandelt. Geschafft hat das die niederländische Firma Uniqure. Diese Woche hat sie die Ergebnisse ihrer neusten Studie bekanntgegeben. Die Resultate übertreffen alle Erwartungen.»
Der «Blick» titelte: «Erstmals Behandlung für Huntington-Krankheit gefunden.»
Artikel stützten sich auf Medienmitteilung
Aufgrund eines Gendefekts sterben bei der Huntington-Krankheit immer mehr Nervenzellen vor allem in einer Hirnregion ab, die Striatum heisst. Sie ist für ein funktionierendes Gehirn essenziell. Meist setzen die ersten Symptome zwischen 30 und 50 Jahren ein. Die Erkrankten können ihre Bewegungen nicht mehr kontrollieren, verändern sich im Wesen und büssen immer mehr geistige Fähigkeiten ein, bis hin zur Demenz. Auch wenn sich einzelne Symptome lindern und die Lebensqualität punktuell verbessern lassen, schreitet das Leiden unaufhaltsam voran und führt nach 10, 20 oder mehr Jahren zum Tod. Ist ein Elternteil betroffen, ist das Risiko für die Kinder, später ebenfalls daran zu erkranken, fifty-fifty.
Die Artikel in der «NZZ» und im «Blick» stützten sich auf eine Medienmitteilung von Uniqure Biopharma. Diese Firma glaubt, dass sie gegen Huntington ein Mittel gefunden hat. Die «NZZ» und der «Blick» glauben es auch. Aber die US-Arzneiaufsicht FDA glaubt es nicht – zumindest der bisher zuständige Bereichsleiter Vinay Prasad.
Millionenteure Spritzen
Die erste von Uniqure entwickelte Gentherapie gegen eine seltene Form der Bluterkrankheit war für die Firma ein grosser Erfolg: «Hemgenix» wurde 2022 in den USA, 2023 in der EU und 2024 in der Schweiz zugelassen. Mit einem Preis von 3,5 Millionen Dollar pro Therapie zählt «Hemgenix» zu den teuersten Medikamenten überhaupt.
Nun will Uniqure den nächsten Coup landen: eine Gentherapie namens AMT-130 gegen die bisher unheilbare Huntington-Krankheit. Um den Nutzen zu beweisen, gleiste Uniqure eine kleine, auf fünf Jahre angelegte Studie in den USA auf, bei der Patienten per Los entweder der Behandlungs- oder der Vergleichsgruppe zugeteilt wurden.
Während «Hemgenix» in den vergleichsweise leicht zugänglichen Leberzellen wirkt, befinden sich die Zielzellen von AMT-130 tief im Gehirn. Die Behandlungsgruppe erhielt deshalb MRI-gesteuert über dünne Katheter drei Spritzen links und drei rechts ins Gehirn. Sechs Patienten erhielten eine niedrige Dosis, zehn eine hohe.
Bei der Vergleichsgruppe dagegen machten die Ärzte bloss kleine Hautschnitte, damit diese Patienten glaubten, sie hätten die Gentherapie erhalten. Die US-Arzneiaufsicht FDA hatte diesen Vergleich verlangt.
Die Medienmitteilung teilte nicht alles mit
Uniqure veröffentlichte am 23. Juni 2022 die erste Zwischenbilanz nach einem Jahr bei den Patienten, welche die niedrige Dosis erhalten hatten – allerdings nur teilweise und nur in Form einer Medienmitteilung.
Etwa zur gleichen Zeit warnte der Chefredaktor des «British Medical Journal», Kamran Abbasi, vor einer von Pharmafirmen gern benützten Medientaktik: «Die Pressemitteilung ist zum Werkzeug der Propagandisten geworden», schrieb er. «Es ist eine Kommunikationsform, die den Unternehmen und ihren Aktionären dient und nicht den Patienten oder den Ärzten.» Medienmitteilungen anstelle der vollständigen Daten zu benutzen, sei ein «Missbrauch der Macht», fand er, «dreist und unredlich».
In der Medienmitteilung ging Uniqure darauf ein, wie sich bei den Behandelten zwei Laborwerte verhielten, die den Krankheitsverlauf widerspiegeln sollen. Einer der Laborwerte hatte sich nach dem Eingriff negativ verändert, der andere positiv, verglichen mit den Patienten, die nur zum Schein behandelt worden waren. Doch dieser Unterschied hätte auch blosser Zufall gewesen sein können.
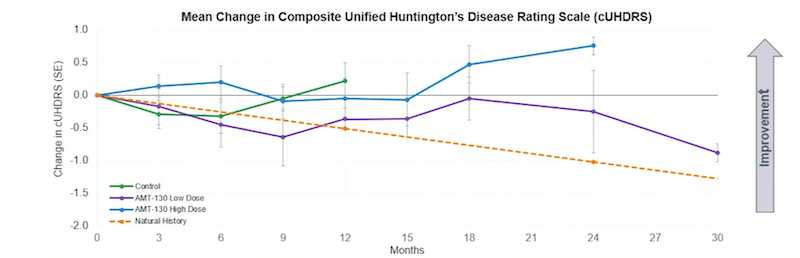
Um den Nutzen der Behandlung zu dokumentieren, wird in der Studie immer wieder verglichen, wie ausgeprägt die Symptome bei den behandelten und bei den nur zum Schein behandelten Patienten sind. Als Mass dient die «Unified Huntington Disease Rating Scale» (UHDRS). Doch in der Medienmitteilung stand nichts von diesen Ergebnissen.
Trotzdem schrieb Uniqure von «exzellentem Fortschritt» im Forschungsprogramm und dass die Firma angesichts dieser 12-Monats-Resultate in der Niedrig-Dosis-Gruppe «ermutigt» sei.
Drei Patienten mit schweren Nebenwirkungen in der Hochdosis-Gruppe
Rund sieben Wochen später musste Uniqure mitteilen, dass es in der Hoch-Dosis-Gruppe bei drei Patienten zu schweren unerwünschten Wirkungen mit lokalen Entzündungen im Gehirn gekommen war, von denen sich die Betroffenen aber «ganz oder teilweise erholt» hätten. Das Experiment mit der hohen Dosis wurde für einige Monate pausiert.
Im Februar 2024 gab ein ranghoher Uniqure-Mitarbeiter an einer wissenschaftlichen Konferenz bekannt, wie sich die Symptome der Patienten verändert hatten: Im ersten Studienjahr zeigte sich im Vergleich mit der Scheinbehandlung kein eindeutiges Bild. Zu diesem Zeitpunkt wussten weder die Patienten noch ihre Ärzte, wer behandelt oder nur scheinbar behandelt worden war.
Allein der Glaube an die Wirkung kann schon helfen
Danach erfuhren sie es. Im Studienplan war diese sogenannte «Entblindung» vorgesehen. Nun gab es ein Problem.
Denn allein der Glaube, eine wirksame Behandlung zu erhalten, kann die Bewegungsstörungen und die geistigen Fähigkeiten der Patienten merklich verbessern – über ein Jahr lang. Das zeigte beispielsweise eine letztes Jahr veröffentlichte Studie in «Neurology». Auch bei der Huntington-Erkrankung wirken demnach Placebo-Effekte.
Etwa ab dem 15. Monat schienen sich in der Hochdosis-Gruppe die Werte deutlich zu verbessern. War dies nun dem Placebo-Effekt geschuldet, weil die Patienten wussten, dass sie eine hohe Dosis erhalten hatten, wirkte die Gentherapie oder war der Unterschied bloss zufällig?
«Ermutigende Daten» – oder falscher wissenschaftlicher Ansatz?
Weil der Vergleich mit der nur zum Schein behandelten Studiengruppe jetzt nicht mehr möglich war, zog Uniqure eine neue Vergleichsgruppe heran, mit «real world Teilnehmern», wie der Uniqure-Mitarbeiter betonte: Es handelte sich um Huntington-Patienten aus anderen Studien, die rund 6 bis 18 Jahre zuvor begonnen hatten. Bei ihnen war der natürliche Krankheitsverlauf beobachtet worden. Uniqure pickte gezielt Patienten heraus, die denen in ihrer eigenen Studie möglichst ähnelten.
Und siehe da: Verglichen mit dem natürlichen Verlauf habe sich die Krankheit innerhalb von zwei Jahren mit der hohen Gentherapie-Dosis relativ um 80 Prozent bremsen lassen und mit der niedrigen Dosis um 30 Prozent – «ermutigende Daten», schrieb der Hersteller in einer weiteren Medienmitteilung im Juli 2024.
«Der hier durchgeführte Vergleich mit historischen Daten aus Beobachtungsstudien […] ist mit einigen Vorbehalten verbunden. In solchen Studien rechnen die Prüfärzte mit einem Fortschreiten der Huntington-Krankheit und neigen viel eher dazu, die Patienten im Verlauf schlechter zu bewerten als in einer klinischen Studie, in der Behandlungseffekte erwartet werden», warnte der globale Studienleiter der AMT-130-Studien, Ralf Reilmann vom George-Huntington-Institut in Münster. Solche Probleme könnten nur gelöst werden, indem man eine Vergleichsgruppe in der Studie habe, die nicht weiss, ob sie behandelt worden sei oder nicht. Oder indem man objektive Messgrössen verwende, bei denen keine Placebo-Effekte auftreten würden. Er sei «sehr begeistert» von den vorliegenden Daten, schrieb Reilmann, «aber wir sollten realistisch sein und die Ergebnisse nicht überbewerten». Auf Anfrage von Infosperber antwortete er bisher nicht.
«Wir hoffen, dass unsere Interpretation korrekt ist»
Uniqure war sich bewusst, dass der Vergleich mit externen Vergleichsgruppen zu falschen Schlüssen führen kann. «Wir hoffen, dass unsere Interpretation korrekt ist. Aber es stimmt: Sicher können wir nicht sein», antwortete der Uniqure-Mitarbeiter auf eine kritische Frage nach seinem Vortrag.
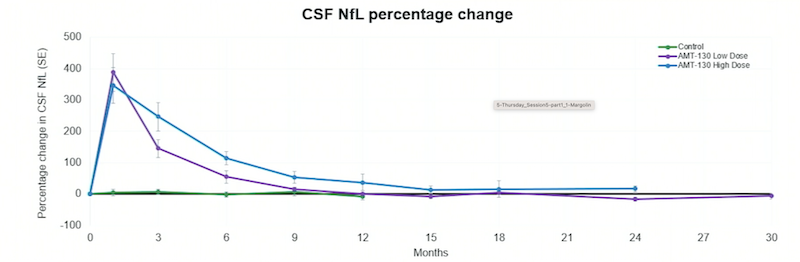
Die Firma untermauerte ihre Aussagen mit einem Laborwert namens CSF NfL. Ist er erhöht, zeigt dies an, dass Nervenzellen untergehen, sei es durch eine Erkrankung oder zum Beispiel einen Eingriff am Gehirn wie bei dieser Gentherapie. Unmittelbar nach den AMT-130-Spritzen stieg der Wert bei den Behandelten stark an, später sank er. In der Hochdosis-Gruppe war er Uniqure zufolge nach 36 Monaten rund acht Prozent tiefer als zu Beginn der Studie. Doch wie stark dieser Laborwert sinken müsse, damit es den Huntington-Patienten erkennbar besser gehe, sei nicht bekannt. Das sagt ein Professor, der namentlich nicht genannt werden möchte. Auch er findet: «Bevor wir uns ein definitives Urteil bilden können, brauchen wir mehr Daten.»
Aktienkurs sackt jäh ab
Für Uniqure, die sich selbst als «führende Gentherapie-Firma» bezeichnet, steht viel auf dem Spiel: Allein in den USA sollen etwa 40’000 Menschen von Huntington betroffen sein, «in der Schweiz sind rund 800 Menschen an Huntington erkrankt, in Deutschland sind es etwa 10’000. Dazu kommen etwa 30’000 Menschen, die das mutierte Gen in sich tragen, bei denen die Symptome aber noch nicht eingesetzt haben», recherchierte die «NZZ» und titelte: «Huntington galt als unheilbar – nun verlangsamt eine neue Gentherapie erstmals den Verlauf.»
Laut einer Schätzung würde jede Behandlungmit AMT-130 mehrere Millionen Dollar kosten. Uniqure strebt eine Zulassung so rasch wie möglich an. Ihr zufolge hatte die US-Arzneimittelbehörde zugesichert, dass sie das Zulassungsgesuch für die Gentherapie beschleunigt prüfen werde. «Wenn alles nach Plan läuft, könnte laut Uniqure die Therapie in den USA bereits im kommenden Jahr angeboten werden», schrieb die «NZZ» im September 2025.
«Ich bin begeistert.» Selbst in ihren kühnsten Träumen hätte sie nicht mit einer so starken Verlangsamung des Krankheitsverlaufs gerechnet, liess sich Sarah Tabrizi, Neurologie-Professorin am University College in London, damals in den Medien zitieren. Sie ist an der europäischen AMT-130-Studie beteiligt. Auf Anfrage von Infosperber jetzt antwortet sie nicht.
Ihr Kollege Edward Wild sagte der «BBC» damals: «Das Ausmass der Wirkung ist atemberaubend.» Jetzt antwortet er auf die Frage nach seinen Erfahrungen mit AMT-130 und weiteren Fragen: «Der regulatorische Aspekt ist sehr heikel und nicht wirklich mein Fachgebiet, daher kann ich dazu leider keine weiteren Angaben machen. Sorry!»
Im ersten Quartal 2026 wollte Uniqure bei der US-Arzneimittelbehörde FDA das Zulassungsgesuch einreichen.
Doch dazu kam es nicht. Denn im November 2025 entschied die FDA: Die vorliegenden Daten genügen nicht für ein Zulassungsgesuch.
Der Geschäftsführer von Uniqure fiel aus allen Wolken. Zumindest äusserte er sich öffentlich so. Uniqures Aktienkurs fiel um 66 Prozent. Die Aussage der FDA habe «Schockwellen durch den Biotechnologie-Sektor gesendet», schrieb das Branchenportal «Fierce Biotech». Das «Wall Street Journal» schimpfte, die FDA habe die Torpfosten verschoben. Die Behörde behaupte, sie wolle für schnellere Arzneimittelzulassungen sorgen, insbesondere bei Krankheiten, bei denen grosse Not herrsche – aber stattdessen tue sie das Gegenteil und blockiere.
Widersprüchliche Ergebnisse, je nach Auswertung
Die FDA dagegen argumentierte: Betrachte man die Daten der Uniqure-Studie ein Jahr nach der experimentellen Behandlung, gebe es keinen Unterschied zwischen den Behandelten und denen, die nur zum Schein «behandelt» worden waren. Folglich hatten die Spritzen ins Gehirn keine Wirkung. Vergleiche man die gleichen Daten aber mit denen der externen Vergleichsgruppe, die Uniqure heranzog, zeigte AMT-130 nach einem Jahr eine Wirkung. Beides passe nicht zusammen.
Aus Sicht von Uniqures Chief Medical Officer sei es «praktisch unmöglich», bei Patienten mit Huntington im frühen Stadium wie in dieser Studie nach nur einem Jahr schon einen Erfolg zu erwarten. Dazu schreite die Erkrankung zu langsam fort, sagte er gegenüber «Fierce Biotech».
Dem Portal zufolge behauptet Uniqure, die FDA habe den Vergleich mit der externen, historischen Vergleichsgruppe vor Jahren selbst genehmigt. Die FDA bestreitet das. Eine solche Zusage sei nie gemacht worden. Die FDA habe immer auf einem direkten Vergleich bestanden. Das sagte ein hoher FDA-Mitarbeiter in einem vertraulichen Gespräch mit Journalisten.
Ungewöhnlich deutliche Worte eines (un-)bekannten FDA-Mitarbeiters
Dort nahm er kein Blatt vor dem Mund: AMT-130 sei gescheitert und aus Sicht der FDA sei der Vergleich mit einer externen Gruppe verzerrt oder manipuliert. Er hielt die von Uniqure vorgebrachten Behauptungen, ihre Gentherapie könne die Behandlung von Huntington «fundamental verändern», für nicht belegt.
Für die FDA geht es um die Frage: Soll sie eine womöglich drei Millionen teure Gentherapie zulassen – ohne klaren Beweis, dass sie den Patienten nützt, und manchen womöglich sogar schadet? Um zu beweisen, dass AMT-130 wirke, verlangt die FDA von Uniqure nun eine grössere Studie mit einer Vergleichsgruppe, die nur zum Schein behandelt wird.
Damit ist die schnelle Zulassung vom Tisch. Am gleichen Tag, als das bekannt wurde, fiel der Aktienkurs von Uniqure erneut – und der Druck auf die FDA stieg. Der Leiter der FDA sprach von einer «Schmierenkampagne». Medien warfen der Behörde vor, sie sei Patienten-feindlich. Im Fokus der Kritik stand der Leiter des Bereichs Biologika, Vinay Prasad.
«Schmierenkampagne» gegen einen, der sich unbeliebt machte
«Diplomatisch» ist nicht das Wort, das Prasad beschreibt. Bevor er zur FDA stiess, sprach er als Medizinprofessor laut aus, was andere nur hinter vorgehaltener Hand flüsterten. Seit Jahren kritisierte er zum Beispiel schlecht gemachte, aber dennoch von den Medien gehypte Studien.
Als 2025 bekannt wurde, dass Prasad zur FDA wechseln würde, sanken die Aktienkurse von über einem Dutzend Biotechfirmen, die Zell- oder Gentherapien auf den Markt bringen wollen. Der «Nasdaq Biotechnologie Index» verlor damals sieben Prozent (Infosperber berichtete).
Er sei aufrichtig, aber kein Teamplayer und bei der FDA angetreten, «das zu tun, wofür er sich sein ganzes Berufsleben lang eingesetzt hatte: die Beweisanforderungen [für Medikamente – Red.] zu erhöhen». So beschrieb ihn der Herzspezialist Anish Koka in seinem Blog auf Substack.
Kaum im Amt, legte sich Prasad mit mehreren Biotechfirmen an, die neue Zell- oder Gentherapien in der Entwicklungspipeline hatten. Unter seiner Leitung lehnte die FDA auch andere Zulassungsgesuche wegen unzureichender Wirksamkeit ab, schob sie auf oder unterbrach die Auslieferung (Infosperber berichtete). In der Zeit vor Prasad hatte die FDA zum Beispiel eine Gentherapie gegen Muskelschwund zugelassen, obwohl ihre eigenen Fachleute selbst nicht glaubten, dass sie wirke. Kostenpunkt: 300’000 Dollar pro Jahr. Nicht nur das «Wall Street Journal» hatte früher kritisch über diese Zulassung berichtet.

Uniqure will Zulassung in Europa beantragen
Die «Schmierenkampagne» im Fall Uniqure endete im März damit, dass ein Journalist den ranghohen FDA-Mitarbeiter, der das vertrauliche Mediengespräch in Sachen Uniqure geführt hatte, in «Stat News» outete. Er nannte zwar den Namen nicht, aber er beschrieb ihn absichtlich so, dass jeder wusste: Es war Vinay Prasad. Noch am selben Tag gab der FDA-Leiter bekannt, dass Prasad die Arzneibehörde per Ende April verlassen werde.
Das «Wall Street Journal» liess gleichentags eine Patientenvertreterin zu Wort kommen, die «regulatorische Flexibilität» forderte. Die Zeitung verlangte, dass die FDA den ablehnenden Entscheid betreffend Uniqure überdenken solle. Andernfalls könnten die Patienten gezwungen sein, nach Europa abzuwandern. Dort will Uniqure nun die Zulassung für AMT-130 beantragen. Und demnächst nochmal das Gespräch mit der FDA suchen.
Themenbezogene Interessenbindung der Autorin/des Autors
Keine
_____________________
➔ Solche Artikel sind nur dank Ihren SPENDEN möglich. Spenden an unsere Stiftung können Sie bei den Steuern abziehen.
Mit Twint oder Bank-App auch gleich hier:
_____________________
Meinungen in Beiträgen auf Infosperber entsprechen jeweils den persönlichen Einschätzungen der Autorin oder des Autors.












Infosperber trifft die negativen Kritikpunkte an der Berichterstattung und an der Evidenzlage von AMT-130 im Wesentlichen gut. Die Therapie ist nicht bewiesen, die Datenlage ist methodisch begrenzt, und frühere Jubelmeldungen gingen deutlich über das hinaus, was die Daten tragen. Problematisch ist aber, dass der Artikel die wissenschaftlich durchaus interessanten Aspekte des Ansatzes kaum würdigt, etwa die biologische Plausibilität, die neuartige intrazerebrale Genregulation und die Tatsache, dass es zumindest ermutigende klinische Signale gibt. Dadurch kippt der Text stellenweise von berechtigter Kritik in eine Art Gegen-PR: nicht mehr nüchterne Korrektur von Übertreibung, sondern ein eigenes, zugespitztes Framing. Und das ist ja das Letzte, was ich mir von einer Berichterstattung wünsche.
Korrigieren Sie mich; Aber eine biologische Plausibilität ist lediglich ein Grund um überhaupt mit forschen zu beginnen, bzw weiterführende Studien zu finanzieren. Es ist letztenendes ein Gedankenkonstrukt das noch belegt werden muss. Und bei wohl jedem Medikament an dem geforscht wird, gibt es eine biologische Plausibilität. Es kann wohl angenommen werden, dass sich biologische Plausibilitäten öfters als Falschannahme denn als korrekt entpuppen. Für eine Zulassung, und darum geht es im Bericht schlussendelich, ist eine biologische Plausibilität völlig irrelevant.
Und ich glaube, wir haben eher zu viel denn zu wenig von solchen Medienmitteilungen die unbewiesenes verbreiten mit der Hoffnung auf steigende Kurse oder eventuell sogar, noch viel schlimmer, als Druckmittel gegen Zulassungsstellen.
@ Herrn Lehmann: Biologische Plausibilität, neuartige Genregulation und die Tatsache, dass es zumindest ermutigende klinische Signale gibt – das gilt genauso für das Beispiel der sehr teuren Gentherapien, die Sarepta auf den US-Markt brachte. Und dann? Die Firma erfüllte Auflagen der FDA nicht, erbrachte die geforderten Studien / Nutzenbelege nach der Zulassung nicht, es kam zu teils schweren Nebenwirkungen usw. Infosperber hat hier und hier darüber berichtet.