Rekord: Ein Preisaufschlag von über 4000 Prozent
Viele Leukämie-Spezialisten waren sauer, als der der französische Pharmakonzern Sanofi im Sommer 2012 den bewährten Infusions-Wirkstoff Alemtuzumab europaweit vom Markt nahm. Einer Patientengruppe dieses Medikament «wegzunehmen» sei «unethisch», sagte Torsten Hoppe-Tichy, Chefapotheker des Universitätsspitals Heidelberg in der ARD-Sendung «Kontraste».
Wenige Monate später wurde das Motiv von Sanofi und deren Tochter «Genzyme» offenkundig. Sie fanden heraus, dass der Wirkstoff Alemtuzumab auch bei Multipler Sklerose MS wirkt. Im September 2013 hat die Europäische Zulassungsbehörde den Wirkstoff für diese neue Indikation bewilligt.
Damit Ärzte nicht auf die Idee kommen…
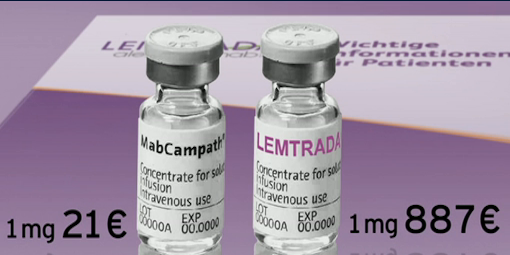
Allerdings verlangt Sanofi für diesen identischen, zwanzig Jahre alten Wirkstoff in Deutschland jetzt 42x mehr als vorher. Damit Ärzte nicht auf die Idee kommen, die günstigen Leukämiespritzen auch bei MS zu verwenden, hat der Pharmakonzern das gegen Leukämie zugelassene Arzneimittel aus dem Markt gezogen und unter dem neuen Markennamen «Lemtrada» für MS-Kranke neu lanciert. Wolf-Dieter Ludwig, Vorsitzender der Arzneimittelkommission der deutschen Ärzteschaft, brandmarkte den neuen Preis in der ARD-Sendung «Kontraste» als «masslos» und kritisierte das «Profitstreben» des Pharmakonzerns.
Swissmedic hat Infosperber bestätigt, dass Sanofi-Genzyme das bisherige Präparat «MabCampath» mit dem Wirkstoff Alemtuzumab für Leukämie-Behandlungen auch in der Schweiz «widerrufen» hat. Falls die Swissmedic den gleichen Wirkstoff in Zukunft für MS-Behandlungen zulässt, wird Sanofi auch von den Schweizer Krankenkassen einen Preis ähnlicher Grössenordnung wie in Deutschland fordern. Das Bundesamt für Gesundheit stützt sich bei der Festsetzung der Preise im Wesentlichen auf einen Auslandspreisvergleich – zu einem erhöhten Euro-Wechselkurs von 1.29, und erst noch mit einem zusätzlichen Aufpreis von ein paar Prozenten. Man darf gespannt sein.
In Deutschland können Pharmafirmen bei neuen Medikamenten die Preise selber festsetzen. Nach einem Jahr wird dann geprüft, ob das Medikament im Vergleich mit der bisherigen Standardtherapie tatsächlich Vorteile bringt. Ist dies nicht der Fall, wird der von den Kassen vergütete Preis auf denjenigen der Standarttherapie gesenkt. Diese Regelung gelte allerdings nicht für alte Wirkstoffe, die für eine neue Anwendung lanciert werden, hiess es in der Sendung «Kontraste». Diese Lücke suchten Pharmakonzerne auszunutzen.
Viel mehr MS-Patienten als Leukämie-Patienten
Abgesehen vom Preis sind Umsatz- und Gewinnaussichten mit Behandlungen von MS-Patienten viel grösser als mit Leukämie-Patienten. In Deutschland gibt es 120’000 MS-Patienten, in der Schweiz etwa 10’000. Viele Patienten sind nicht viel älter als dreissig Jahre alt.
Sanofi erklärte in der Sendung «Kontraste», dass die Behandlung von MS-Patienten mit dem «neuen» Medikament «nach zwei kurzen Behandlungsphasen abgeschlossen» sei. Diese zweimal fünftägigen Infusionen im Abstand von einem Jahr kosten zusammen pro Patient 85’000 Euro. Diesen Preis hält Sanofi für «angemessen», weil bisherige Medikamente bei MS ähnlich teuer seien.
Professor Bernhard Hemmer vom «Klinikum rechts an der Isar» in München, der Erfahrungen mit Alemtuzumab sammeln konnte, meinte, dass zwei Behandlungsphasen wahrscheinlich nicht reichten. Zudem würden etliche Patientinnen und Patienten die Behandlung vorzeitig abbrechen, weil sie an zu starken Nebenwirkungen litten.
In den USA noch nicht zugelassen
Die Zulassung des früheren Leukämie-Mittels für die Behandlung von MS-Kranken ist in den USA umstritten. Das zuständige Beratungsgremium der Zulassungsbehörde FDA kam zu verwirrenden Schlüssen, wie die Ärzte-Webseite «Medscape» am 13. November berichtete. Es lohnt sich, die Zusammenfassung im Original zu lesen:
The US Food and Drug Administration’s (FDA’s) Peripheral and Central Nervous System Drugs Advisory Committee today gave the new multiple sclerosis (MS) drug alemtuzumab (Lemtrada, Genzyme) a roller coaster ride, not reaching definite conclusions at the end of the day as to whether it should be approved or not.
Despite voting 11 to 6 (with 1 abstention) that the 2 pivotal trials — known as 323 and 324 or CARE-MS I and CARE-MS II — were not adequate or well controlled, the panel then voted 12 to 6 in favor of the sponsor having provided adequate evidence of effectiveness.
To add to the confusion, the panel voted 14 to 2 (2 abstentions) that the sponsor had not provided sufficient evidence of alemtuzumab on reduction of disability, but voted 17 to 0 (1 abstention) that, assuming efficacy results are as they appeared, safety results would not preclude approval.
Finally, the panel voted 16-0 (2 abstentions) that if the drug were approved, it should not be indicated as a first-line agent.
Panel chairman, Nathan Fountain, MD, University of Virginia, Charlottesville, acknowledged that the panel came to no strong resolution.
Dem Nutzen stehen Nebenwirkungen gegenüber
Die «Deutsche Multiple Sklerose Gesellschaft», die Alemtuzumab grundsätzlich positiv beurteilt, warnt immerhin vor folgenden Nebenwirkungen:
«Die häufigsten Nebenwirkungen sind infusionsbedingte Reaktionen, Infektionen (der oberen Atemwege und der Harnwege) und Verminderung von weißen Blutkörperchen (Lymphopenie und Leukopenie). Außerdem kann es bei Patienten unter Lemtrada® zu schwerwiegenden Autoimmunstörungen kommen. Ein umfassendes Risikomanagementprogramm soll zur Früherkennung und zum frühzeitigen Management solcher Autoimmunerkrankungen beitragen.»
—
Nachtrag
Warum gibt es für diesen fast 20-jährigen Wirkstoff keine Nachahmerprodukte? Der Neurologe Professor Gavin Giovannoni von London erklärt über die Nachahmung des gentechnisch hergestellten Biosimilars Alemtuzumab Folgendes: «Unlike small molecules it is very difficult to make copies of biologicals (protein-based therapeutics). In addition, the FDA and EMA expect clinical trials to make sure the biosimilar has the same effects as the innovator drug. So even if it comes off patent the hurdle for making a rip-off drug is very high and unlikely to happen.»
—










Teile der Familien Rockefeller, Rothschild, Carnegie, Harriman, Morgan, Schiff und Warburg, ihnen gehört über 90% des Weltkapitals. Der Rest der Welt muss buhlen, einige bleiben auf der Strecke, der Stärkere gewinnt. Es gibt Politiker die sagen, dass der derzeitige Kapitalismus tötet, sei der normale, natürliche Preis einer funktionierenden, wachsenden, blühenden Marktwirtschaft. Das ist die Ursache für solche Preisexzesse, tiefer kann man nicht mehr gehen. Preisüberwachung ist dringendst notwendig, doch auf Dauer braucht es von Grund auf eine komplette Neu-Regulierung der kapitalistischen Demokratie. Denn ansonsten bringt die zunehmende Plutokratie die Demokratie ganz zum verschwinden. Wer so was wie ich hier schreibt, wird schnell mal in die Verschwörungstheorie-Ecke abgeschoben, aber ich schreibe keine Bücher darüber. Ich lese nur gerne mal die Times, die NZZ und andere Zeitungen und schaue mir die Zahlen an, dann wird alles klar.
Man vergisst gerne mal, dass auch für neue Indikationen neue klinische Teststudien notwendig werden, die entsprechend teuer sind. Wenn man nur mit dem Preis konfrontiert wird, vergisst man das gerne mal. Ändert allerdings nichts am moralischen Aspekt.
Ja da haben Sie recht. Und eben, die wirtschaftlichen Voraussetzungen um in einem moralisch vertretbaren Bereich zu bleiben sind absolut nicht gegeben.
Bonjour,
Meine Muttersprache ist Fr, probiere ich trotzdem auf deutsch.
Ich habe seit sehr kurzer Zeit ein merkwürdiges Buch gefunden, das diese Themen klar beschreit. Von den 1950 Jahren bis heute. Der Titel ist: Bigpharma, und der Author ist MIKKEL BORCH- JACOBSEN. Editor: Les Arènes, auf français .